富士通研究所と富士通は、グラフ構造のデータを学習する富士通研究所独自のAI技術Deep Tensorと学術文献など専門的な知識を蓄積したナレッジグラフを関連付けることにより、大量のデータを学習させたAIの推定結果から、推定理由や学術的な根拠を提示する技術を開発した。
同技術は2018年度に富士通株式会社のAI技術「FUJITSU Human Centric AI Zinrai」での実用化が予定されている。
Deep Learningは高い認識・分類性能が得られる一方で、なぜその答えが出てきたのかを専門家や開発者自身が説明できないため、ブラックボックス型のAIと呼ばれている。
このような性質は、AIを使った専門家の判断に関して説明責任が問われるミッションクリティカルな領域への適用の妨げになると懸念されており、ブラックボックス型のAIに説明機能を持たせる技術の開発が期待されてきた。
そこで今回、同社は独自のAI技術であるDeep Tensorと様々な外部データから構築したナレッジグラフを関連付けることで、Deep Tensorの推定理由や根拠を提示する技術を開発した。推定結果に大きく影響した因子(部分グラフ)を特定し、ナレッジグラフの部分グラフと対応付け、これらをナレッジグラフ上でつなぐ形で、一連の情報を推定根拠として構成する。
ゲノム医療における専門家の調査作業の効率化を想定した模擬実験として、生物情報学分野における公開データベースや医療文献データベースを用いた学習データとナレッジグラフを利用して、関係性が部分的にしか知られていないような事象に関して裏付けとなる根拠を探し出し、紐づけ可能かどうかの検証を行った。
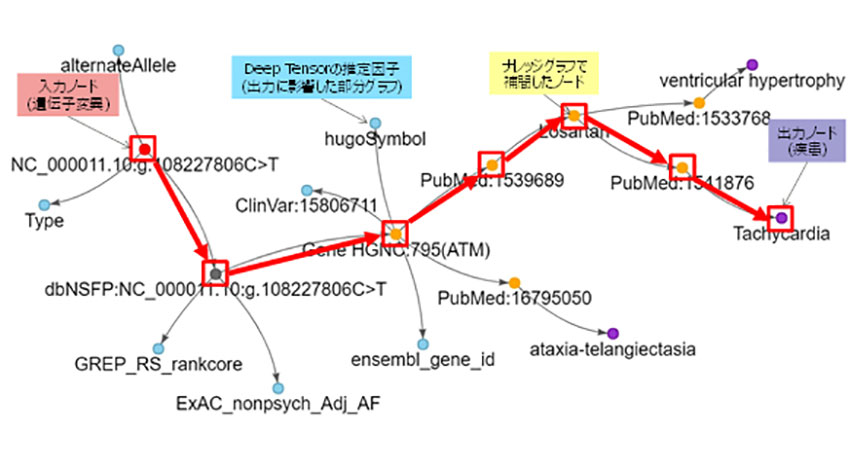
公開データベースから構築した遺伝子変異と病因性の関係について学習し、推定に影響した因子や根拠について学術論文や関連情報を抽出した結果では、推定対象の遺伝子変異(赤)について、推定結果に大きく影響した複数の因子(青)とナレッジグラフから取り出した医療文献などからなる学術的な裏付けとなる根拠(黄)および疾患の候補(紫)を同時に見ることができた。
今後は、医療に係わる研究機関の協力を得て、今回の技術によって示された根拠が専門家にとって意味があるか、十分にわかりやすいかという点の検証をしていくという。また、金融分野における融資先の自動推定を学習させた場合に規制や規則の知識を用いて推定の妥当性を確認するなど他分野への応用も計画している。
なお、効果検証に用いたデータの一部は、国立研究開発法人日本医療研究開発機構(AMED)「臨床ゲノム情報統合データベース整備事業」における「ゲノム医療を促進する臨床ゲノム情報知識基盤の構築」に関し、国立大学法人京都大学との共同開発により得られた成果によるものだ。
今回開発された技術は、以下の2つの技術より構成されている。
- 推定因子特定技術
Deep Tensorでは、同じデータでも様々な表現方法があるため学習が困難だったグラフ構造のデータについて、グラフ構造のデータからテンソルと呼ばれる数学表現への変換方法の学習とDeep Learningの学習を同時に行うことで、グラフ構造のデータの高精度な学習を可能にする。
今回、個々の入力データについてのDeep Learningの出力結果から逆に探索して、推定結果に大きく影響した複数の因子を入力データの部分グラフとして特定する技術を開発。同技術では、Deep Learningの入力となるテンソル間の類似性に基づき個別の推定結果の決め手となる要素を抽出し、さらにテンソルからグラフ構造のデータへの逆変換により抽出した要素に対応する入力の部分グラフを特定する。
- 根拠構成技術
推定に大きく影響した複数の因子はナレッジグラフと関連付けることで、それぞれの因子に関連する情報を特定できる。そこからグラフ構造を辿って関連する知識を得る事ができるが、ナレッジグラフは様々な情報の様々な関連性をグラフ構造で保持しているため、単純にグラフ構造を辿るだけでは推定理由と無関係な情報を関連付けてしまう問題があった。
同技術では複数の推定因子を手掛かりとしてグラフ構造を探索することにより、特定された推定因子に関連性の高い情報だけを抽出し、根拠として構成する。
提供:富士通研究所、富士通
【関連リンク】
・富士通研究所(FUJITSU LABORATORIES)
・富士通(FUJITSU)
・国立研究開発法人日本医療研究開発機構(AMED)
・京都大学(Kyoto University)
無料メルマガ会員に登録しませんか?

技術・科学系ライター。修士(応用化学)。石油メーカー勤務を経て、2017年よりライターとして活動。科学雑誌などにも寄稿している。




















