タンパク質は非常に柔軟で、さまざまな形態を取り得ることで、生体内の他の分子と相互作用している。
例えば、ヒトに感染するウイルスが体内に侵入するには、ウイルス表面のタンパク質の形態が変化して細胞表面のタンパク質と結合するため、感染を抑制する薬を効率的に設計するには、ウイルス表面におけるタンパク質の多様な変化の形態を知ることが重要となる。
しかし、タンパク質はそれぞれの原子が3次元の座標を持ち、原子数×3の次元を持つ高次元データとなる。このような高次元空間で、標的タンパク質の広範囲な構造変化の情報を得るには、高度な専門知識と試行錯誤が必要であり、長い期間と多くの費用が必要であった。
この課題解決に向けて、富士通株式会社と国立研究開発法人理化学研究所(以下、理研)計算科学研究センター(R-CCS)HPC/AI駆動型医薬プラットフォーム部門は、独自の生成AI技術とスーパーコンピュータ「富岳」で処理した大規模な画像データを活用することで、「生成AI技術」と「構造変化を予測する技術」の、二つの新たな技術を開発した。
これは、生成AIを活用し、大量の電子顕微鏡画像からタンパク質の構造変化を広範囲に予測できるAI創薬技術だ。標的タンパク質の大量の電子顕微鏡の画像から、その立体構造の多様な形態と、それらが取り得る割合を正確に推定する生成AI技術および、推定された割合から、標的タンパク質の構造変化を予測する技術を開発した。
通常、タンパク質の広範囲な構造変化を予測するためには、最初に構造の割合を推定し、次に、構造の時間変化を正確に推定するという2つのステップの推定を実現する必要がある。
そこで、富士通独自の生成AI技術「DeepTwin(ディープツイン)」と、理研の創薬分子シミュレーションの知見を応用して開発した二つの技術を活用して、標的タンパク質の構造変化の予測を、従来の1日から2時間に短縮することが可能となった。(※タンパク質合成にかかわるタンパク質であるリボソームデータを今回の技術に適用した場合の効果。)
具体的には、さまざまな方位からの多様な形態が映し出された大量の電子顕微鏡像を生成AIの学習に用いることで、3D密度マップそのもののデータがなくても、タンパク質の構造変化分析が可能な低次元の潜在分布を獲得する生成AIを開発した。
この生成AIモデルでは、歪み理論にもとづき数学的に証明したところ、撮影画像数が十分であれば、下図②と同一の分布(下図①)を低次元空間内で平易な数式として得ることができる。
つまり、この技術に大量の電子顕微鏡画像を適用すれば、従来は得ることが困難であったタンパク質の各形態の割合を間接的に高精度に推定することができる。
また、標的タンパク質のある瞬間をとらえた大量の投影画像と投影角から、投影対象を組み立てる計算をして、立体構造の多様な形態を3D密度マップとして復元すると同時に、復元された立体構造の各形態への変化の頻度を手掛かりに、標的タンパク質が取り得る形態の割合を、実験データに基づく形で見積もることを可能にした。
さらに、低次元化された特徴量を用いて、化学分野で使われる反応経路の分析を適用可能にする技術を開発。低次元での分析結果を、独自の生成AIにより元の高次元データに復元することで、標的タンパク質の構造変化の予測を実現した。
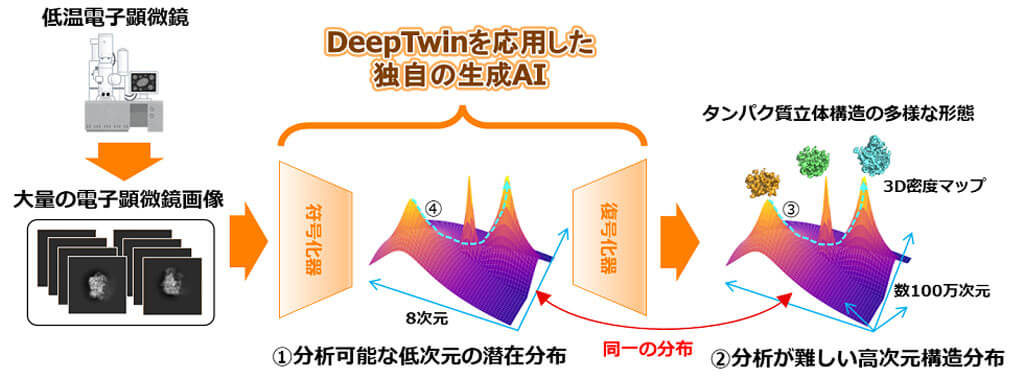
この技術では、タンパク質のある形態から別の形態への構造変化予測を、本来の高次元空間の本質的な情報を保存した低次元の潜在空間を介すことにより、実現している。
まず、前項の生成AIモデルの訓練(上図)を通して得られる低次元の潜在分布上で、平易な数式を基に最適経路(上図④の水色破線)を求める。
次に、得られた低次元の変化列を、復号化器を用いて高次元化し、3D密度マップの変化列に変換する。
これにより、これまで困難であったタンパク質の構造変化の予測を可能とした。また、撮影画像が十分な場合、技術が予測する構造変化は、タンパク質の最適反応経路(前述方程式の解)と等価になることを数学的に示されている。
この技術は、従来の標的タンパク質の構造変化列の構成手順に比べて、10倍以上高速に大量の電子顕微鏡画像からタンパク質の形態と構造変化の推定が可能になるため、細菌やウイルスなどの標的タンパク質に結合する薬剤の設計過程を支援することが期待できる。
両者は今後、今回開発した生成AI技術を、標的タンパク質と抗体の複合体解析や分子の大域的な構造変化を、高精度かつ高速に予測するIT創薬技術を実現するためのコア技術のひとつとして活用していくとしている。
また、富士通は、タンパク質の構造変化の予測技術を、先端技術を素早く試せるAIプラットフォーム「Fujitsu Kozuchi(code name)-Fujitsu AI Platform」のAIイノベーションコンポーネントとして、2023年10月10日より提供開始する。
さらに、それら二つの技術を基に、タンパク質の構造変化を3D密度マップの連続的な変形として予測できるAI創薬技術を開発した。なお両者は、この技術に関する論文を、2023年10月10日(日本時間)に、医療用画像処理分野のトップ国際会議「MICCAI 2023」で発表した。

IoTに関する様々な情報を取材し、皆様にお届けいたします。